lunes, 29 de octubre de 2012
Teoría Molecular de la materia
Teoría Cinético-Molecular
domingo, 28 de octubre de 2012
Estados de la materia.
Como ya se dijo anterior
mente la teoría cinética de la materia explica los estados de agregación que
son:
SOLIDO: Sus partículas están
muy próximas entre sí y vibran sin desplazarse. Las fuerzas de atracción entre
las partículas son elevadas y sus oscilaciones se hacen mayores al elevar la
temperatura
 LÍQUIDO: Sus partículas no ocupan
posiciones fijas. Los líquidos toman la forma del recipiente que los contenga.
Sus fuerzas de atracción son menores que las de un sólido.
LÍQUIDO: Sus partículas no ocupan
posiciones fijas. Los líquidos toman la forma del recipiente que los contenga.
Sus fuerzas de atracción son menores que las de un sólido.  GASEOSO: Las partículas están
muy alejadas y las fuerzas de atracción son muy pequeñas, de igual manera que
los líquidos toman la forma del recipiente que lo contenga
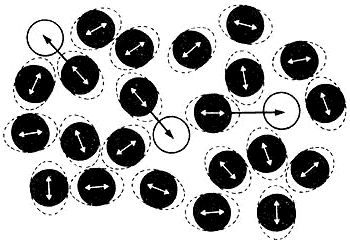
GASEOSO: Las partículas están
muy alejadas y las fuerzas de atracción son muy pequeñas, de igual manera que
los líquidos toman la forma del recipiente que lo contenga
En esta página podrás encontrar la definición y características de cada uno de los estados de agregación , así como algunos ejercicios que te recomendamos resuelvas.
Concepto
DILATACIÓN Y SU EXPLICACIÓN EN LA TEORÍA
CINÉTICA
(DILATACIÓN:
Incremento de volumen que experimenta un sistema material al aumentar su
temperatura)
La dilatación es
un concepto indispensable en la Teoría Cinética ya que en esta se explica
claramente de la siguiente forma: "Al calentar un sistema material,
aumenta su temperatura y la agitación de sus partículas, sea un sólido, un
líquido o un gas. Al moverse más rápidamente, las partículas necesitan de un
mayor espacio o volumen y por ello el sistema material se dilata"
Los gases se
dilatan más que los líquidos, y estos más que los sólidos.
Todos los
estados pueden lograr tener una dilatación aunque en los sólidos son cuantitativamente menos importantes pero aun así
no se pueden ignorar.
Este fenómeno se
puede definir mediante la siguiente formula física:
Y su definición
es:
“LA DILATACIÓN VOLUMÉTRICA QUE SE PRESENTA EN
UN LIQUIDO ES DIRECTAMENTE PROPORCIONAL A LA DIFERENCIA DE VOLÚMENES E
INVERSAMENTE PROPORCIONAL AL VOLUMEN INICIAL MULTIPLICADO POR LA DIFERENCIA DE
TEMPERATURAS”
Dulce Maria, Cabrieza.
"Física y Química", México, Editex, 2007, p.37.
sábado, 27 de octubre de 2012
Introducción a la teoría cinética de
los gases:
La teoría cinética de los gases se basa en dos
hechos fundamentales:
♦la molécula es
la parte más pequeña en que se puede dividir una sustancia sin perder
sus características y propiedades.
♦Las moléculas de
los gases están en continuo movimiento. Hay varios hechos que
contribuyen a demostrar esta afirmación, los más importantes son:
-Un gas ocupa siempre todo el volumen del recipiente que lo
contiene.
-Los fenómenos de difusión de gases solo son
explicables por el movimiento de sus moléculas.
-El movimiento browniano,
que aunque descubierto en coloides, es decir,
en partículas en suspensión en líquidos, contribuyo a
desarrollar la teoría que permite determinar el número de Avogadro.
Se entiende por presión de un gas, el impulso que
las moléculas de gas trasmiten por su choque con la superficie del
recipiente que lo contiene.
Dos masa cualesquiera se hayan sometidas a una fuerza atractiva
llamada también newtoniana, constituyendo la llamada Ley
de Gravitación Universal. Las moléculas de gas por el hecho
de tener masa deberían estar sometidas a esta fuerza atractiva, sin
embargo la teoría cinética postula que "entre las moléculas
de un gas, las fuerzas de origen newtoniano son nulas, por lo que
las únicas variaciones que puede sufrir su
velocidad corresponden a los
intercambios energéticos producidos en los choques
totalmente elásticos que ocurran.
La hipótesis de Avogadro afirma que a condiciones normales
(temperatura y presión) un mol de cualquier gas ocupa el mismo volumen, el llamado volumen molar, y se completa
afirmando que tiene el mismo número de moléculas, número que se llama de
Avogadro y cuyo valor es: N(A)= 6,023.10 23
moléculas/mol.
Esto nos indica que el número de moléculas de un gas es tan
elevado, que a las magnitudes que las atañen individualmente, trayectoria,
velocidad, etc., es imposible agregarle otros conceptos que los meramente
estadísticos, es decir, dado el elevadísimo número de elementos que constituyen
las moléculas de un gas, solo es posible acudir para su estudio, a magnitudes
estadísticas.
"Temas de Física", ECU, López
Vázquez Luis B., pag. 323-324.
LA
TEORÍA CINÉTICA DE LA MATERIA.
A lo largo de la historia
del pensamiento humano se ha elaborado un modelo acerca de cómo está
constituida la materia, se conoce con el nombre de MODELO CINÉTICO-MOLECULAR.
Con este modelo, puede
explicarse perfectamente el hecho de que la materia pueda encontrarse en tres
estados: SÓLIDO, LÍQUIDO y GASEOSO.
La TEORÍA CINÉTICA DE LA MATERIA, supone que la materia sea cual se su
estado de agregación está formado por moléculas que están en movimiento e interactúan
entre sí.
La teoría cinética ayuda a explicar
las propiedades de la materia en términos de fuerza entre las moléculas y la energía
que tienen.
Los tres postulados básicos
de la teoría son:
-La materia está compuesta
de partículas muy pequeñas, llamadas moléculas. Las propiedades químicas de la
materia dependen de su composición. Las propiedades Físicas por ejemplo
dependen de la fuerza que las moléculas ejercen entre si y la distancia que las
separe.
-Las moléculas están en
constante movimiento. El promedio de la energía cinética de las moléculas depende
de la temperatura.
-Las moléculas obedecen las
leyes de movimiento de Newton. En los choques entre las moléculas su momento
lineal y su energía cinética no cambia.
González Cabrera,Víctor Manuel. Física Fundamental, Ed.Progreso. pag. 101,102
viernes, 26 de octubre de 2012
Introducción al blog
Bienvenidos a nuestro blog "Aprende la Teoría Cinética" , éste es creado por alumnos de bachillerato de la E.N.P Núm. 7 "Ezequiel A. Chávez", está a cargo de los siguientes integrantes del grupo 607:
Calvario Yáñez Paulina
Casillas Cuevas Nareny
Díaz Huerta Rodrigo
Fuentes García Israel
Gonzalez Amaro Karen
Trujillo Sánchez Jordan
Nuestra Profesora: Antonia María Teresa Díaz Martínez
Materia: Física IV
Aquí encontrarás definiciones, conceptos fundamentales, ejemplos, experimentos, videos, entre otros materiales interesantes que te ayudarán a comprender la Teoría Cinética.
Nuestra finalidad es aprender a realizar trabajos de investigación sobre un tema especifíco, así mismo comprender este tema mediante la búsqueda de documentos reelevantes y también ayudar a jóvenes con dudas sobre dicho tema con nuestros archivos.
Suscribirse a:
Comentarios (Atom)